Inteligencia Artificial
La Cofepris autoriza medicamento para tratamiento del VIH y otro biotecnológico para leucemia aguda linfoide

La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) autorizó 25 medicamentos, entre ellos, una molécula nueva para el tratamiento del VIH, y un biotecnológico para la leucemia aguda linfoide.
Dio a conocer que, de acuerdo con el más reciente Informe quincenal de ampliación terapéutica, de la primera mitad de julio, se autorizaron 149 insumos para la salud en las categorías de medicamentos, dispositivos médicos y ensayos clínicos.
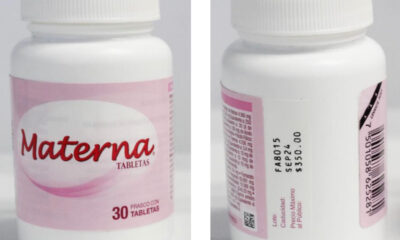
Precisó que el nuevo medicamento contra el Virus de Inmunodeficiencia Adquirida (VIH) es el efavirenz/lamivudina/tenofovir disoproxil fumarato y el biotecnológico para la leucemia aguda linfoide el L-asparaginasa.
Lee: Tras riguroso análisis, Cofepris autoriza más de 7 millones de cajas de clonazepam y metilfenidato

Los Cabos detonan a la industria del turismo de reuniones en México: FITURCA

Ana Torroja: 40 años arriba y debajo del escenario abriendo brecha a las mujeres

La skater Sofía Guerrero Salcido desafía la adrenalina para conquistar medallas

“No debemos alejarnos de la sociedad”: Ricardo Monreal

En Sonora la cotización del dólar afecta el precio de la aguamala
El organismo señaló que también obtuvieron registro sanitario 116 nuevos dispositivos médicos, de los cuales 21 son para atención médica, entre ellos audífonos auxiliares auditivos, un sistema cerrado de drenaje de heridas, un sistema de placas y tornillos de osteosíntesis y prótesis total de rodilla y de hombro.
Aclaró que 35 son equipos médicos, como un kit de anestesia subdural, medidores de glucosa en sangre, un videolaringoscopio flexible e instrumental para prótesis de cadera.
Indicó que 60 equipos son para medición de hemoglobina glicolizada, función hepática, hormonas, cobre, zinc, antígeno p24 para detección de VIH, toxina de tétanos, trypanosoma cruzi y actor reumatoide, entre otros.
De acuerdo con la Cofepris, también se autorizaron ocho nuevos ensayos clínicos: tres para medicamentos para el tratamiento de cáncer, uno para niños mayores de 12 años y adultos con hemofilia A o B grave y un protocolo para determinar los efectos del tratamiento para VIH en personas con obesidad.
Agregó que a través de la labor de su Comisión de Autorización Sanitaria (CAS), cumple con garantizar el acceso a insumos para la salud, sometidos a estricta revisión y dictamen que comprueba su seguridad, calidad y eficacia, necesarios para la obtención del registro sanitario.
La generación y publicación del Informe quincenal de ampliación terapéutica es un ejercicio pleno de transparencia de esta autoridad hacia las industrias reguladas y los pacientes, objetivo central de una regulación sanitaria ágil, justa y transparente.
Lee: La Cofepris liberará los medicamentos psiquiátricos fabricados por Psicofarma después del 11 de mayo


 Zacatecashace 11 horas
Zacatecashace 11 horasSe celebra en Fresnillo la Tercera Copa Nacional de BMX

 CDMXhace 17 horas
CDMXhace 17 horasEn el Estado de México existen condiciones seguras para las elecciones: secretario de Seguridad

 Viajes360hace 18 horas
Viajes360hace 18 horasEsta es la fiesta de la Santa Cruz, en Los Realejos, el pequeño pueblo de las Islas Canarias, en España

 Negocioshace 21 horas
Negocioshace 21 horasLa banca mexicana se mantiene sólida gracias a sus políticas sanas: S&P Global Ratings

 Inteligencia Artificialhace 14 horas
Inteligencia Artificialhace 14 horasEl tamaulipeco Roberto Cantoral trascendió fronteras con sus composiciones musicales

 Seguridadhace 23 horas
Seguridadhace 23 horasEl PRD propone otorgar seguro de vida a las y los policías de entidades federativas y municipios

 Viajes360hace 12 horas
Viajes360hace 12 horasEl Callejón de Miguel Barragán es Patrimonio Histórico poco reconocido por los xalapeños

 Guanajuatohace 22 horas
Guanajuatohace 22 horasLa soprano de la Universidad de Guanajuato, Carolina Herrera destaca entre las mejores óperas de México